El riego con agua embotellada comercial incrementa la generación de especies reactivas del oxígeno en Nicotiana tabacum
Noviembre, 2020
Marissa Calderón-Torres, Edith López-Estrada, Ana E. Ortiz-Reyes1 & Miguel Murguía-Romero
Resumen
El consumo de agua embotellada comercial se ha incrementado a nivel mundial de manera sorprendente. Para asegurar que su consumo no tenga efectos dañinos en la salud humana, se debe realizar investigación. Se analizó el crecimiento de plantas de Nicotiana tabacum después de ser regadas con agua de la llave y embotellada comercial. Las plantas irrigadas con agua embotellada comercial tuvieron menor número de hojas, algunas con clorosis, y tuvieron una longitud más corta de tallo y hoja en comparación con las plantas irrigadas con agua de la llave, y además su raíz, tallo y hoja mostraron un aumento en la producción de especies reactivas del oxígeno y una disminución significativa de clorofilas. El análisis químico del agua embotellada comercial mostró una concentración baja de iones y un valor de pH ácido (5.5) por debajo del mínimo de la norma mexicana NOM-127-SSA1-2000 (6.5–8.5). El crecimiento, la concentración de clorofila y la capacidad antioxidante de las plantas regadas con agua embotellada se ven afectados negativamente en comparación con las regadas con agua de la llave.
Palabras clave: Nicotiana tabacum, agua comercial embotellada, clorosis, especies reactivas del oxígeno.
Introducción
A nivel mundial hay un aumento en el consumo de agua embotellada y México es uno de los principales países con mayor consumo [1]. La introducción del agua comercial embotellada en México se debió históricamente a la escasez del agua, para cubrir necesidades urgentes durante desastres naturales, para proveerla a la población en ciudades de zonas desérticas, así como a la presencia de microorganismos patógenos en el agua para beber [3,4].
El alto consumo de agua comercial embotellada ha llevado a la investigación de los siguientes tres aspectos esenciales: i) la composición mineral y orgánica, así como también contaminantes microbiológicos y radioactividad, porque estos pueden causar serios efectos en la salud humana [5]; en el caso del agua embotellada en México se han encontrado residuos de pesticidas organoclorados, radioactividad alfa y presencia de microorganismos patógenos como coliformes, todos estos sobrepasando los límites permitidos para el consumo humano [6,7,4]; ii) el método de desinfección del agua, pues los componentes derivados pueden reaccionar con iones orgánicos disueltos en el agua tales como compuestos halógenos o nitrosaminas que se han reportado en el agua para consumo humano [8,9]; finalmente, iii) el tipo de plástico en el que el agua es embotellada, que ha recibido especial interés porque el tipo de plásticos de policarbonato y las resinas empleadas para su elaboración [10] pueden causar la liberación de diferentes elementos y compuestos orgánicos a la comida o al agua [11] que pueden afectar el sistema endocrino humano [12]. Por ejemplo, se ha encontrado antimonio (Sb) y ftalatos en agua comercial embotellada de la ciudad de Monterrey, México, su presencia se deriva del plástico polietileno tereftalato (PET) usado para las botellas del agua y ambos son considerados tóxicos y elementos dañinos para el ambiente [13,14].
En la mayoría de estos trabajos de investigación el objetivo es determinar si la calidad del agua que se pretende para consumo humano cumple con los estándares establecidos en la legislación del país correspondiente para asegurar que no hay riesgo para la salud humana. Sin embargo, la evaluación directa de los efectos del consumo prolongado de agua comercial embotellada en humanos es escasa, probablemente porque los efectos sobre la salud son variables, y dependen del tiempo en que se manifiestan los primeros problemas de salud, que puede variar de meses a años. Por lo tanto, se prefiere el uso de organismos vivos, como plantas o animales, en el estudio de enfermedades o terapias, debido a la capacidad de respuesta o evolución a los cambios en su entorno [15]. Las plantas se usan ampliamente para monitorear la contaminación del ambiente y, entre las plantas usadas para este propósito, las del tabaco han probado ser útiles [16]. Se ha demostrado recientemente que la expresión genética y la actividad específica de enzimas del metabolismo central de N. tabacum, por ejemplo, la malato NADP+ oxidoreductasa, son sensibles a diversos factores estresantes abióticos, tales como los cambios de salinidad, temperatura, pH y sequía, entre otros [17,18].
Hay tres hechos que muestran la necesidad de investigación de los efectos adversos para el humano del consumo de agua embotellada. Primero, la investigación de la calidad del agua para beber que evalúa los riesgos en la salud de los mexicanos se ha enfocado sólo en el análisis de componentes minerales y orgánicos, así como contaminantes radiactivos y biológicos. Segundo, hay pocos estudios enfocados a evaluar los efectos del agua comercial embotellada para beber en organismos vivos. Y finalmente, hay un alto consumo de agua comercial embotellada en México.
Para evaluar los posibles efectos en la salud del agua comercial para beber uno puede empezar por investigar los efectos adversos en modelos animales o de plantas. Las plantas son modelos adecuados porque tienen un ciclo de vida relativamente corto y se han usado para investigar los efectos de contaminantes. En este trabajo se evalúa el crecimiento de plantas de Nicotiana tabacum irrigadas con agua comercial embotellada por 55 días comparándolo con el de plantas irrigadas con agua de la llave, midiendo parámetros morfológicos y bioquímicos.Material y Métodos
Las plantas se cultivaron de acuerdo a [19]. La germinación y crecimiento de Nicotiana tabacum se hizo en el Jardín Botánico de la Facultad de Estudios Superiores Iztacala, U.N.A.M. Previo a la germinación, las semillas de la planta Nicotiana tabacum recibieron un tratamiento de escarificación con NaCIO (4%) y se colocaron en un tamiz con luz de malla de 10 mm, luego se lavaron con agua destilada estéril. Después se colocaron en suelo estéril (tierra previamente filtrada con un tamiz de luz de malla de 3 mm) y se incubaron en condiciones estándar de crecimiento a 25 °C, humedad relativa del 35% y un ciclo de luz/obscuridad de 12 hrs. Después de tres semanas, las plántulas se transplantaron a tierra estéril (filtrada con un tamiz de luz de malla de 1 cm).
Las plantas se dividieron en dos grupos de riego de cinco plantas cada uno: i) agua de la llave de la Alcaldía Miguel Hidalgo, Ciudad de México y ii) agua comercial embotellada para consumo humano. Las plantas se crecieron por 55 días y se regaron cada tercer día con 10 mL de cada tipo de agua. Al final del crecimiento se midió la longitud y el ancho de las hojas y la longitud del tallo. Una muestra de la raíz, tallo y hoja de cada planta se colocó en tubos Eppendorf de 1.5 mL y se congelaron con nitrógeno líquido para su almacenamiento a -70 °C.
Figura 1. Nicotiana tabacum después de crecer con dos tipos de agua. Las plantas se irrigaron por 55 días cada tres días con a) agua de la llave (n=5) y b) agua comercial embotellada (n=5).
Extractos celulares totales de Nicotiana tabacum
Para preparar los extractos celulares, se tomaron 100 mg de muestra de cada raíz, tallo y hoja y se colocaron en tubos Eppedorf de 1.5 mL, a cada tubo se añadió 300 mL de amortiguador salino de fosfatos (PBS por sus siglas en inglés) 10 mM y 3 mL de fluororo de fenilmetilsulfonilo (PMSF) 100 mM y las muestras se homogeneizaron con un micro pistilo de teflón a 4 °C. Luego los tubos se centrifugaron a 16,000 x g, 5 min a 4 °C. El sobrenadante se trasfirió a un nuevo tubo Eppendorf y se incubó a 4 °C. La concentración de proteínas en el extracto celular se determinó mediante una curva estándar de proteína de albumina de suero bovino (BSA).
Producción de especies reactivas del oxígeno (ERO) en Nicotiana tabacum
Los niveles de ERO en cada uno de los tres tejidos de la planta que se analizaron (raíz, tallo y hoja) se determinaron empleando el método de [20], se prepararon tres muestras de cada una de las cinco plantas para cada tejido de cada uno de los grupos experimentales, es decir, 90 lecturas en total. Este método se basa en la reacción del peróxido de hidrógeno con el compuesto diacetato de 2ʹ7'-diclorodihidrofluoresceína (DCFH-DA), que produce 2’7’-diclorofluoresceína con emisión de fluorescencia. Las reacciones se hicieron en una placa de 96 pozos; a cada pozo se añadió 20 mL del extracto celular, 225 mL de PBS 10 mM y 5 mL de DCFH-DA (500 mM). Las lecturas de emisión se registraron cada 20 min por 1 hora en un espectrofotómetro de fluorescencia (Bio Tek) a 485 nm de excitación y 520 nm de emisión. El valor máximo de fluorescencia que se obtuvo en cada serie de tiempo se utilizó como índice de la producción de ERO por mg de proteína total.
Cuantificación de clorofilas
Las clorofilas se midieron mediante el método de [21]. Primero, se tomaron 100 mg de hoja de cada planta y se colocaron en un tubo Eppendorf de 1.5 mL, luego se añadió 100 mL de acetona (80%) y la mezcla se maceró con un micropistilo de teflón. El macerado se transfirió a un tubo Falcón de 15 mL y se diluyó con 2 mL de acetona (80%), el tubo se agitó en vórtex y se centrifugó a 500 x g 10 min. En una celda de cuarzo se añadió 1 mL de extracto de clorofilas y se registró la lectura de absorbancia en un espectrofotómetro a 645 y 663 nm. Los datos de absorbancia que se obtuvieron en cada longitud de onda se utilizaron para calcular la concentración de clorofilas en mg/mL.
Capacidad antioxidante de Nicotiana tabacum
La capacidad total antioxidante en las hojas de Nicotiana tabacum se determinó mediante un sistema comercial (Cayman Chemical, No. 709,001). El sistema se sustenta en una reacción de oxidación en la que la enzima metmioglobina y el peróxido de hidrógeno (H2O2) producen la oxidación del ácido 2'2-azino-bis-[3-etilbenzotiazol-6-sulfónico] (ABTS) con un cambio de color; sin embargo, los antioxidantes presentes en los extractos celulares previenen la oxidación de ABTS. En este trabajo, en lugar de usar la enzima metmioglobina, se empleó la enzima peroxidasa (Pepro Tech). La capacidad antioxidante de los extractos celulares se determinó mediante una curva estándar de TROLOX, este compuesto es un análogo del tocoferol o vitamina E. Las reacciones de oxidación se hicieron en una placa de 96 pozos, a cada pozo se añadió 10 mL del extracto celular (volumen ajustado a una concentración de proteína total de 1.5 mg/mL), 10 mL de la enzima peroxidasa, 40 mL de peróxido de hidrógeno y ABTS. La lectura de absorbancia de la placa se hizo en un espectrofotómetro a 405 nm. La capacidad antioxidante se expresó en equivalentes de la concentración molar de TROLOX.
Muestreo del agua
El agua embotellada para beber de una marca comercial se compró en tiendas de venta al por menor (n = 3) de la Alcaldía Miguel Hidalgo de la Ciudad de México y el agua de la llave se colectó en una toma domiciliaria de la misma área (n = 3). Al momento de la compra de las botellas de agua, se verificó que la fecha de expiración fuera al menos de seis meses en el futuro. Los protocolos para la colecta, preservación y transporte de las muestras de agua de la llave y la embotellada se hicieron siguiendo los procedimientos descritos en [22]. Después de la colecta, inmediatamente todas las muestras se transportaron al Laboratorio de Química Analítica del Instituto de Geofísica, U.N.A.M. (laboratorio especializado en el análisis de agua) y se guardaron en refrigeración hasta su análisis.
Análisis químico del agua
La composición química del agua de la llave y de la embotellada se determinó por triplicado en el Laboratorio de Química Analítica del Instituto de Geofísica, U.N.A.M. El análisis incluyó la determinación de pH, conductividad (ms/cm), cationes de sodio, potasio, calcio y magnesio, así como iones de carbonato, sulfato, cloro, boro y nitrato (mg/L). Este laboratorio especializado llevó a cabo todos los análisis químicos de acuerdo a los procedimientos estándar establecidos por la Asociación Estadounidense de Salud Pública [23] y descritos en [24].
Cuantificación de Na+ y K+ en Nicotiana tabacum
La determinación de Na+ y K+ se hizo tal como se describe en un trabajo previo [19]. Una muestra de 200 mg de tejido de raíz, tallo y hoja de las cinco plantas de cada grupo de riego se deshidrató en un horno de secado a 80 °C por 48 horas. Luego, cada muestra fría se pesó y colocó en un tubo de ensayo de vidrio de 15 mL y se le añadió 10 mL de agua milli Q. Los tubos fueron incubados en un baño de agua hirviendo por 1 hora, después de su enfriamiento a temperatura ambiente, los tubos se centrifugaron a 1800 x g 10 min. El sobrenadante se transfirió a un tubo Falcón de 15 mL. La determinación de cada ion se hizo con 1 mL del sobrenadante en un fotómetro de flama (Zeiss PF5). Como estándar de cada ion, se empleó una solución de NaCl 1 mM y KCl 1 mM. A partir de las lecturas en fotómetro de flama, se calculó la concentración de sodio y potasio que se expresó como mol/L.
Análisis estadístico
Se obtuvo el valor promedio y error estándar de la media (SEM) de cada determinación. La significación estadística de las diferencias entre los dos grupos de riego se evaluó con la prueba t de Student.Resultados
Parámetros morfológicos de N. tabacum irrigada con agua de la llave y agua embotellada
El tamaño promedio de las hojas de las plantas fue significativamente diferente (Tabla 1). El largo de las hojas de las plantas y regadas con agua comercial embotellada fue más corto comparado al de las hojas de plantas regadas con agua de la llave (longitud 7.1 cm vs. 10.5 cm), también la longitud del tallo fue significativamente diferente (7.8 vs. 12.3 cm). El número promedio de hojas fue más alto en las plantas regadas con agua de la llave (10.6 vs. 8.0). Además se observó clorosis en las hojas de plantas crecidas con agua comercial embotellada (Figura 1).
Producción de ERO y capacidad antioxidante en extractos celulares de N. tabacum
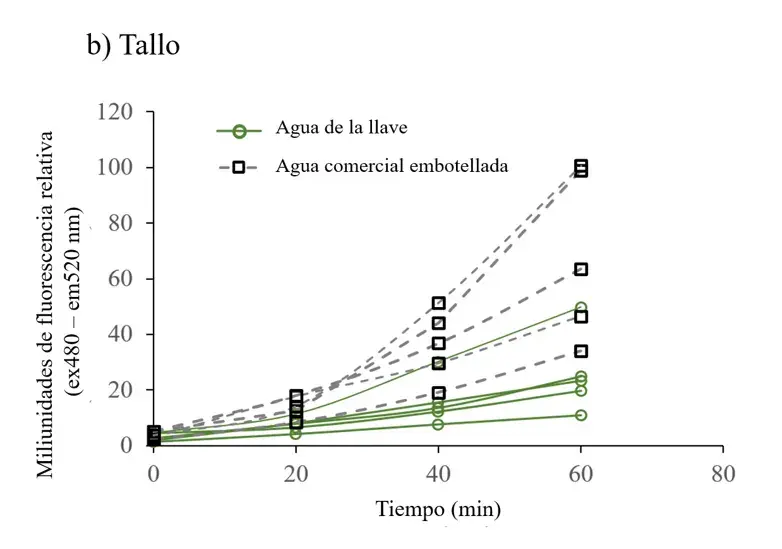
Para determinar si la clorosis observada en hojas de plantas crecidas con agua comercial embotellada correlacionaba con la producción de radicales libres, se midió la concentración de las especies reactivas del oxígeno en todas las plantas. En las plantas regadas con agua comercial embotellada los niveles de ERO incrementaron en el tiempo en todas las estructuras de la planta (Figura 2), esto fue particularmente significativo en el tallo (Figura 3a).
Respecto a la capacidad antioxidante, las hojas de plantas irrigadas con agua comercial embotellada exhibieron una reducción de sistemas antioxidantes comparada con las plantas irrigadas con agua de la llave (Figura 3b).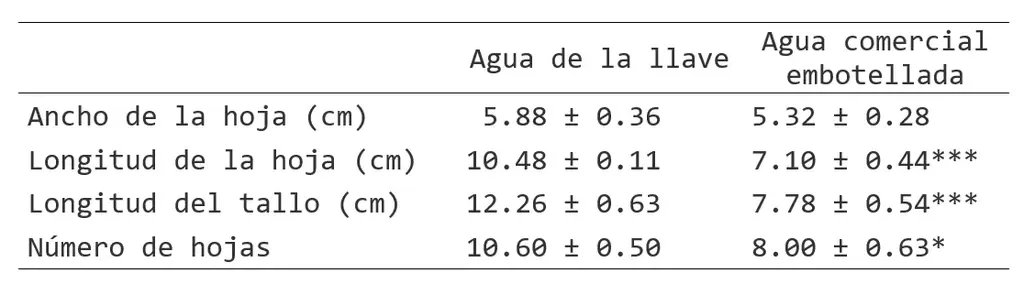
Tabla 1. Mediciones morfológicas de tallo y hoja de plantas irrigadas con agua de la llave y agua comercial embotellada. Valores promedio ± SEM; n=3. * P<0.05, ***P<0.001.
Figura 2. Series de tiempo de fluorescencia de ERO de extractos celulares de raíz (a), tallo (b) y hoja (c) de plantas irrigadas con agua de la llave y agua comercial embotellada.
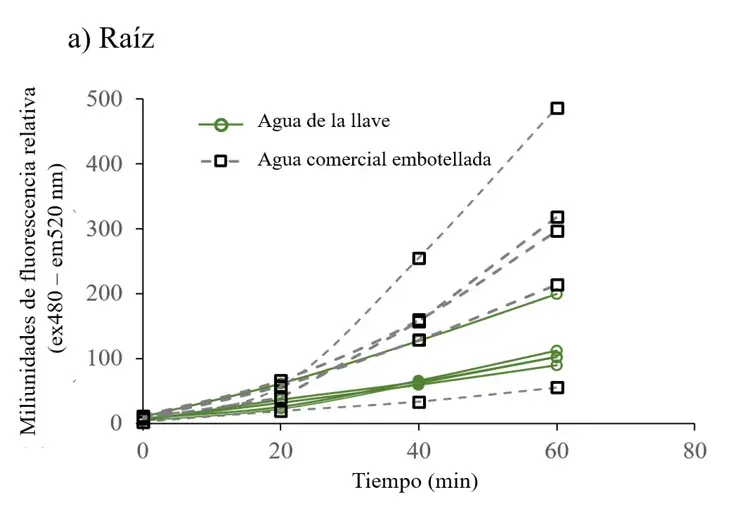
Los extractos celulares fueron leídos con 10 M DHFC-DA y la fluorescencia (excitación a 485nm y emisión a 520 nm) se registró cada 20 min por 60 min. Las diferencias en fluorescencia fueron más claras a los 60 minutos: a) datos de fluorescencia de ERO en extractos celulares de raíz, b) tallo y c) hoja. Cada dato de fluorescencia es el promedio de tres lecturas y fue ajustado a la concentración total de proteína. Cada línea representa los datos de una planta.

Iones solubles Na+ y K+ en Nicotiana tabacum
Para explorar posibles causas de la clorosis se cuantificó la concentración de iones de sodio y potasio en raíz, tallo y hoja. La concentración de Na+ mostró un incremento significativo en raíz y hojas de plantas irrigadas con agua comercial embotellada (Figura 4a), mientras que hubo una concentración más alta de sodio en el tallo de plantas irrigadas con agua de la llave.
Las plantas irrigadas con agua comercial embotellada tuvieron concentraciones más altas de potasio (Figura 4b). Esta diferencia fue estadísticamente significativa en raíz y hoja.
Cuantificación de clorofila A, B y total
Para corroborar si las hojas de las plantas mostraban un cambio en la proporción de clorofila se midió su concentración. Las hojas de plantas irrigadas con agua comercial embotellada tuvieron concentraciones bajas de clorofilas A, B y totales comparadas con la concentración de plantas irrigadas con agua de la llave. Las diferencias fueron significativas para la clorofila A y total (Figura 3c).Figura 3. ERO, capacidad antioxidante y clorofilas en Nicotiana tabacum.
a) Especies reactivas del oxígeno (ERO) en raíz, tallo y hoja de plantas irrigadas con agua de la llave y agua comercial embotellada; b) capacidad antioxidante en hoja; c) clorofilas A, B y totales en hoja (n=5 para cada grupo). Las barras de error representan el error estándar de la media. *P < 0.05.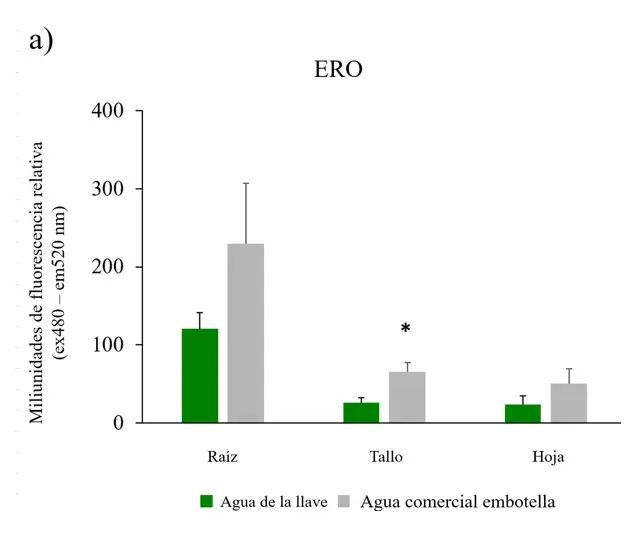
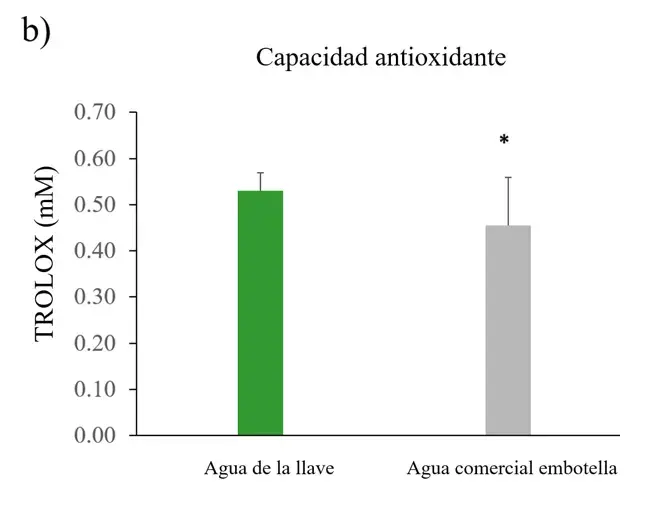
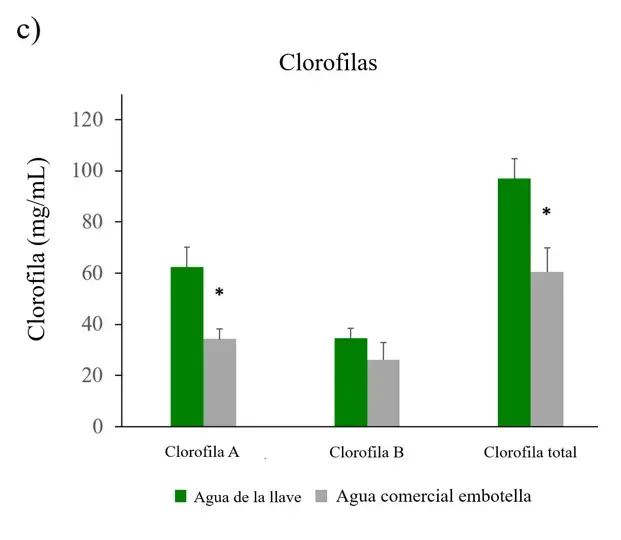
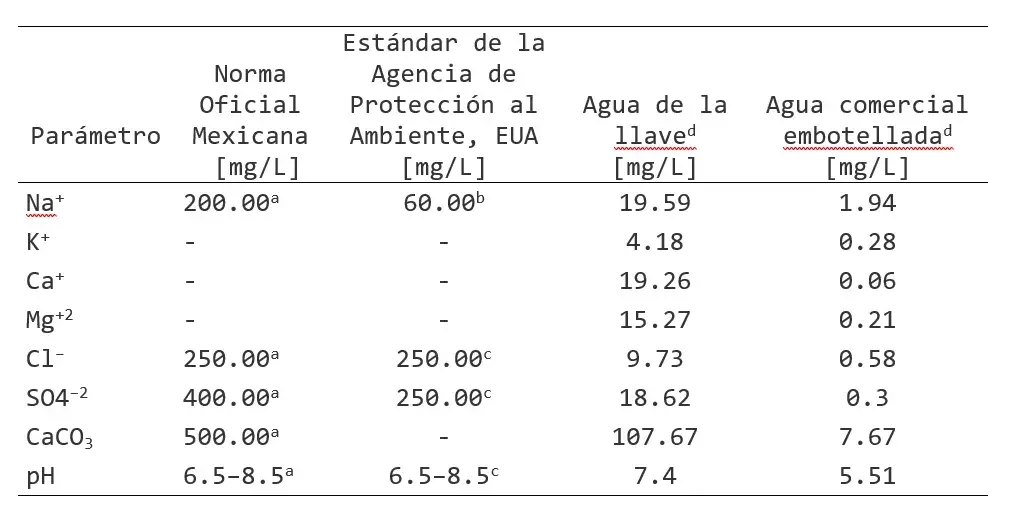
Tabla 2. Composición química básica del agua usada para irrigar a Nicotiana tabacum.
a) Límite máximo permitido de acuerdo al estándar de la NOM-127-SSA1-2000 en México;
b) Concentración límite recomendado para sabor;
c) Límite máximo permitido de la regulación secundaria de la calidad del agua de la agencia de Protección al Ambiente Estadounidense EPA 822-F-18-001 2018 Drinking water standars and health advisories tables;
d) Concentración promedio; n=3.
Análisis químico del agua
Discusión
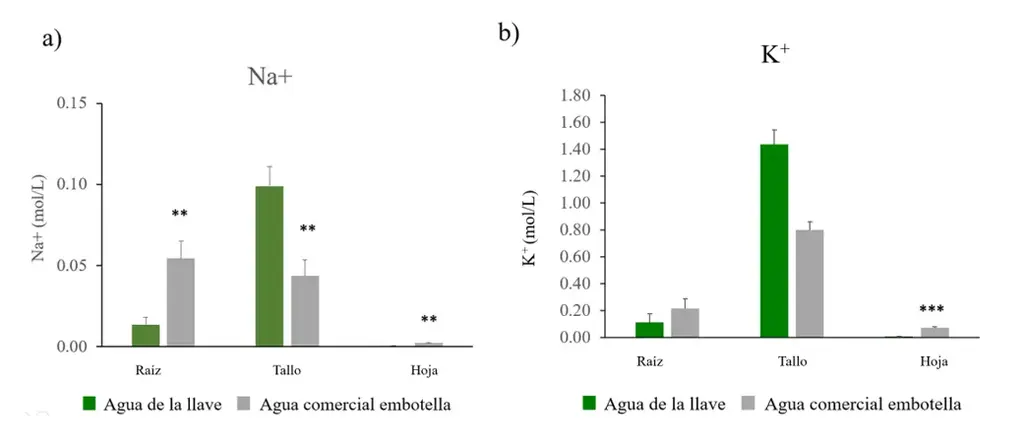
Figura 4. Concentración de Na+ and K+ en Nicotiana tabacum después de ser irrigada con agua de la llave y agua comercial embotellada. Cuantificación de a) sodio, y b) potasio en raíz tallo y hoja de plantas de cada grupo: agua de la llave (n=5) y agua comercial embotellada (n=5). Las barras representan el error estándar de la media. **P < 0.01, ***P <0.001.
Se ha demostrado que bajo diversas condiciones de estrés cómo sequía, inundación, heladas, incremento de salinidad, etc., la clorofila se degrada, lo que conduce a la clorosis en las hojas [26] con subsecuente pérdida de estas. Sin embargo, este hecho es sólo la punta del icebrg, es decir, la clorosis es la consecuencia del estrés.
Entonces, el siguiente paso de este trabajo fue investigar el estrés celular que lleva a la degradación de la clorofila y en consecuencia a clorosis, para ello se consideró que en diferentes condiciones de estrés un factor común es la sobreproducción de especies reactivas del oxígeno (ERO) y nitrógeno (ENO) [27,26] con la pérdida de la capacidad antioxidante, resultando en daño a biomoléculas [29,30]. Por ello, en este trabajo se midió la producción de ERO mediante su reacción con el compuesto diacetato 2ʹ7’-dichlorodihidrofluoresceína (DCFH-DA), normalmente usado para cuantificar H2O2 [31, 32] y los tres tipos de tejidos analizados de plantas irrigadas con agua comercial embotellada tuvieron niveles elevados de ERO. En los extractos de hojas de estas plantas también se cuantificó la capacidad antioxidante y se observó su disminución.
En general la capacidad antioxidante se evalúa mediante la reacción de la enzima comercial metmioglobina y peróxido de hidrógeno (H2O2), que oxidan al ABTS, pero esta reacción se evita con los antioxidantes presentes en los extractos celulares. Sin embargo, en este trabajo la reacción se llevó a cabo con la enzima peroxidasa y H2O2, la oxidación de ABTS también ocurre y se forma el radical ABTS+. Pero si en los extractos celulares están presentes las enzimas catalasas, el peróxido se transforma a agua y oxígeno, ello disminuye la formación de ABTS+ [33]; por lo tanto, un valor bajo de absorbancia corresponde a una mayor concentración de TROLOX, es decir, una alta capacidad antioxidante. Medir la capacidad antioxidante con la enzima peroxidasa también indica la formación de peróxido y en los extractos celulares de las hojas de las plantas con riego de agua de la llave, se observó la mayor concentración de TROLOX, ello significa que las enzimas antioxidantes están degradando H2O2. En contraste, los extractos celulares de las hojas de las plantas con riego de agua comercial embotellada presentaron una menor concentración de TROLOX y niveles elevados de ERO, esto probablemente corresponde al daño de enzimas antioxidantes, que son las encargadas de la degradación del anión superóxido y del peróxido de hidrógeno.
Para verificar la presencia de peróxido de hidrógeno y de catalasas en los extractos celulares, proponemos que en estudios posteriores se mida el peróxido de hidrógeno mediante la actividad de neutralización de radicales en presencia de un agente secuestrante, por ejemplo, el ácido cafeico [34], que actúa como un antagonista del peróxido de hidrógeno mediante la donación de átomos de hidrógeno para reducir el peróxido de hidrógeno a agua. Y para determinar la presencia de la enzima catalasa en plantas, proponemos medir la capacidad antioxidante en presencia y ausencia de un inhibidor de la enzima catalasa como el compuesto 3-amino-1,2,4 triazol, que se ha empleado en adipocitos para desequilibrar el sistema de defensa antioxidante al aumentar la concentración de H2O2 [35].
Las plantas tienen normalmente mecanismos eficientes para neutralizar ERO [36], si disminuye la concentración de las moléculas y enzimas antioxidantes y aumentan las especies reactivas del oxígeno, ocurre un desbalance entre la producción de ERO y la capacidad antioxidante. La sobre producción de ERO es potencialmente perjudicial para las proteínas y lípidos en los cloroplastos. Por lo tanto, se considera que el riego con agua comercial embotellada conduce a una condición severa de estrés oxidante con un aumento de ERO que se asocia a la clorosis que se observó en las hojas.
Es claro que los niveles bajos de potasio en el agua comercial embotellada pueden ser un factor clave en la clorosis de las hojas así como la concentración baja de potasio observada en el tallo de estas plantas. En el caso del magnesio este catión es un componente clave de las moléculas de clorofila que participan en la absorción de la luz. Algunos estudios han reportado que la deficiencia de Mg+2 dispara la clorosis de las hojas; se ha propuesto recientemente un mecanismo en el que se produce ERO vía fotooxidación debido a una acumulación de carbohidratos y falla de fijación de CO2, que a su vez puede acelerar la transferencia de electrones fotosintéticos al O2 y potenciar la producción de ERO [40,41]. En segundo lugar, el pH ácido del agua puede cambiar las características del suelo y en consecuencia cambiar diversas funciones de las plantas. Al inicio de la irrigación con agua comercial embotellada es probable que la composición del suelo amortigüe el pH ácido del agua así como dentro de la célula, pues se ha demostrado que el pH del citoplasma de las plantas en condiciones normales es de 7.5, es decir, ligeramente alcalino [42,43]. Sin embargo, después de riego prolongado con agua con pH ácido es muy probable que el balance del pH del suelo se altere con efectos en la fisiología de la planta. Ya ha sido probado que la exposición corta de suelos o medios de crecimiento a pH ácido puede modificar la permeabilidad de la raíz, por ejemplo, la actividad de proteínas acuaporinas especializadas en el transporte de agua en la raíz se puede reducir y consecuentemente modificar el transporte de nutrientes y agua de la raíz a la hoja [44,45]. Así, la exposición prolongada a pH ácido puede reducir el crecimiento de la planta y esto puede ser el caso de las plantas irrigadas con agua comercial embotellada. Tanto la deficiencia mineral como el pH ácido del agua pueden ser la causa del incremento de la producción de ERO, la reducción de clorofila y, en consecuencia, el tamaño pequeño de las plantas.
Proponemos que en estudios posteriores se examine, en diferentes estados de crecimiento de la planta, la concentración de marcadores de estrés oxidante como el malondialdehído y 3-nistritirosina. Para examinar la acumulación de compuestos derivados de hidrocarbonos se puede evaluar la formación de ERO por ensayo de dithiotreitol [46]. Además, se puede cuantificar la expresión de la enzima malato NADP+ oxidoreductasa como sensor de cambio en el pH del suelo.
Conclusiones
Referencias
Resultados destacados